Nature | 陈晓伟/李蓬/郭强发现内质网蛋白CLCC1感应膜平衡并控制脂流向
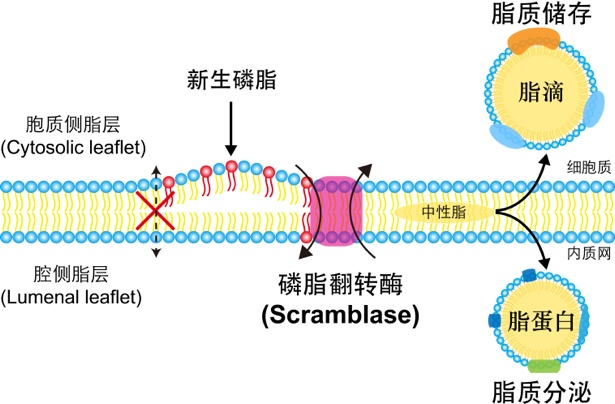
脂质是生命体核心的能量来源和结构组成,其合成、吸收、储存和运输的精密调控对细胞与机体的稳态至关重要;上述过程的失衡,是心血管、神经退行等重大疾病的普遍诱因。细胞内质网是脂质合成的核心场所,亦是脂质命运决定的起点。在内质网双层膜中,磷脂合成呈现跨膜不对称性:其初始合成发生于胞质侧脂层(cytosolic leaflet),随后需翻转至腔侧脂层(lumenal leaflet),方可完成生物膜的组装。中性脂(如甘油三酯等)则在内质网膜脂层之间生成;其胞质流向促成脂滴、从而介导脂质储存,而其腔内流向则可支撑脂蛋白的生成和运输、进而控制血脂(图一)。然而,脂质生成后面临的取向选择及其调控,一直以来是细胞生物学领域的难题,其失衡后的致病机制亦未能明晰。
北京大学陈晓伟团队长期聚焦血脂调控,从人类罕见遗传病(乳糜微粒滞留症)入手,鉴定出维系脂蛋白分泌的特异受体SURF4、并解析其开启的高效可控的血脂运输通路【1,2】;同时借助该通路的膜、脂动态,纯化发现了领域长期探寻的磷脂翻转酶TMEM41B【3】,其肝脏缺失可导致剧烈的代谢病变;上述的系列工作,引发了“脂层不平衡反应”参与构建细胞稳态的猜想【4】,进而提示了脂层失衡感知、脂质分配调控等科学问题。
2026年2月25日,北京大学陈晓伟团队、郑州大学/清华大学李蓬团队、北京大学郭强团队,在Nature合作发表了题为CLCC1 Governs ER Bilayer Equilibration to Maintain LipidHomeostasis的研究论文,鉴定出内质网膜稳态关键感应因子 CLCC1,并阐明其调控脂质分配的分子机制。
陈晓伟团队此前发现,磷脂翻转酶TMEM41B的缺失会导致细胞中异乎寻常的脂质累积。本研究进而结合李蓬团队在脂滴领域的长期积累、借助郭强团队打造的冷冻电子断层扫描(cryo-ET)及多模态光学及电镜成像体系,出人意料的发现TMEM41B缺失导致了脂质的极端错置:磷脂堆积在胞质侧,驱动内质网膜高度卷曲、剧烈失衡;而中性脂则取向腔内,并形成大量被内质网双层膜包裹的异化巨型脂滴(giant-ER enclosed lipid droplets, geLD)。
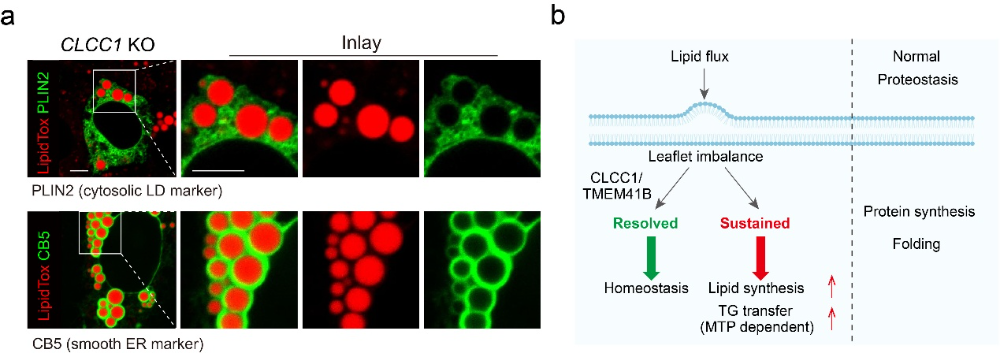
研究者进而推测:大规模出现的失衡脂层,可能成为脂层维稳蛋白质机器的“陷阱”,并可依托geLD实现生化分离、从而捕捉原本高度动态的调控因子。进一步的整合蛋白组学和CRISPR功能验证发现:内质网CLCC1的缺失亦诱发geLD和脂层失衡(图二左),复现了TMEM41B缺失导致的细胞稳态失衡。
遗传分析发现人类CLCC1基因多态性和血脂水平高度相关,小鼠模型中失活肝脏CLCC1亦导致禁食血脂水平几近清零,体现了该基因在机体脂稳态调控中的核心功能。生化实验显示CLCC1与TMEM41B相互作用、并可稳定后者;病理研究进一步提示两者均为细胞及器官稳态所必须。尤为有趣的是:CLCC1可发生诱导性的聚合,进而定位至失衡脂层,提示了其感知脂层失衡、招募效应因子、维持脂层动态平衡的工作模型(图二右)。
值得一提的是,Nature同期发表了UC-Berkeley 的James A. Olzmann团队与Ana Paula Arruda团队的合作论文CLCC1 Promotes Hepatic Neutral Lipid Flux and Nuclear Pore Complex Assembly。该研究利用遗传筛选的手段,同样发现了CLCC1调控脂质取向和脂代谢稳态的核心功能,并同时报道了CLCC1(及TMEM41B)的缺失诱发核膜结构及功能的紊乱。鉴于核膜本质上是内质网膜的特化区域,两项背靠背发表的工作从不同技术路径出发,互为印证,从而提示了内质网脂层平衡调控在决定脂质流向、维系细胞稳态中的基础性作用,为未来研究提供了众多可能。有趣的是,CLCC1的突变可导致渐冻症【5】 ;此外,陈晓伟团队与西湖大学季哲剑团队的合作,以及ETH-ZurichUlrike Kutay/Madhav Jagannathan合作团队,分别通过预印本报道了CLCC1为人类罕见疾病基因ATP酶Torsin的关键底物【6,7】,进一步凸显了上述机制的病理意义。


