郭强团队揭示真核生物核糖体RNA扩展片段介导核糖体二聚休眠的新机制
近日,实验室郭强团队在Nucleic Acids Research杂志在线发表了题为“rRNA expansion segments mediate ribosome dimerization as a conserved stress response”的研究论文。该研究利用冷冻电子断层扫描成像(cryo-ET)技术,在细胞原位解析了核糖体的翻译活性与空间分布形式,揭示了动物细胞中核糖体通过rRNA扩展片段形成二聚体的分子机制,并阐明该过程是一种保守的应激响应,参与翻译调控。
核糖体是由蛋白质和核糖体RNA(rRNA)构成的大型分子机器,承担着细胞内全部蛋白质合成的核心功能。蛋白质合成是细胞中能量消耗最高的过程之一,因此在受到外界胁迫时,细胞往往会迅速降低整体翻译水平。在细菌中,除了对单个核糖体翻译活性的调控外,细胞还可在环境应激条件下依赖休眠因子促使核糖体形成二聚体,从而实现更高层次的翻译调控[1]。这种休眠状态有利于核糖体的储存和保护,维持核糖体群体的稳定性,并在应激解除后促进翻译的快速恢复[2]。然而,真核细胞中是否存在类似的、通过调控核糖体空间拓扑组织来调节翻译活性的机制,长期以来尚不清楚。
在本研究中,利用cryo-ET对大鼠神经元进行原位观察,并结合研究组此前开发的邻近分子拓扑分析方法NEMO-TOC[3],发现应激诱导条件下核糖体会形成两种无活性的二聚体结构(图1)。值得注意的是,这两种二聚体中的核糖体相互作用分别由 rRNA 扩展片段ES31b,以及 ES30a和ES20a介导,并通过 “kissing-loop”方式实现二聚化;这一机制随后又在生化实验中得到了进一步验证(图1E)。rRNA扩展片段是真核核糖体特有的rRNA序列,其在进化过程中具有显著的序列差异,因此长期以来常被视为核糖体中的“结构性冗余”区域,相关功能研究相对有限[4]。本研究首次表明,特定的rRNA扩展片段可在应激条件下直接介导核糖体二聚化。此外,研究还发现,这种核糖体二聚化现象在嘌呤霉素处理、氨基酸缺乏以及内质网应激等多种条件下均可发生,并在应激解除后迅速消失,显示出明显的动态可逆性。
值得一提的是,在本研究审稿期间,Science杂志发表了题为“Ribosomal RNA expansion segments mediate the oligomerization of inactive animal ribosomes”的相关研究[5]。该工作进一步证明,核糖体二聚体对于维持细胞在应激状态下的存活具有重要作用。与 Science 论文仅报道由ES31b介导的一种二聚体结构相比,本研究还进一步发现了另一种由ES30a和ES20a介导的核糖体二聚体。结合研究组此前在U2OS细胞中发现的由ES27L介导的核糖体二聚体[6],这些结果共同提示:rRNA扩展片段的不同区域可能通过介导休眠核糖体二聚体的形成,广泛参与真核细胞的翻译调控。
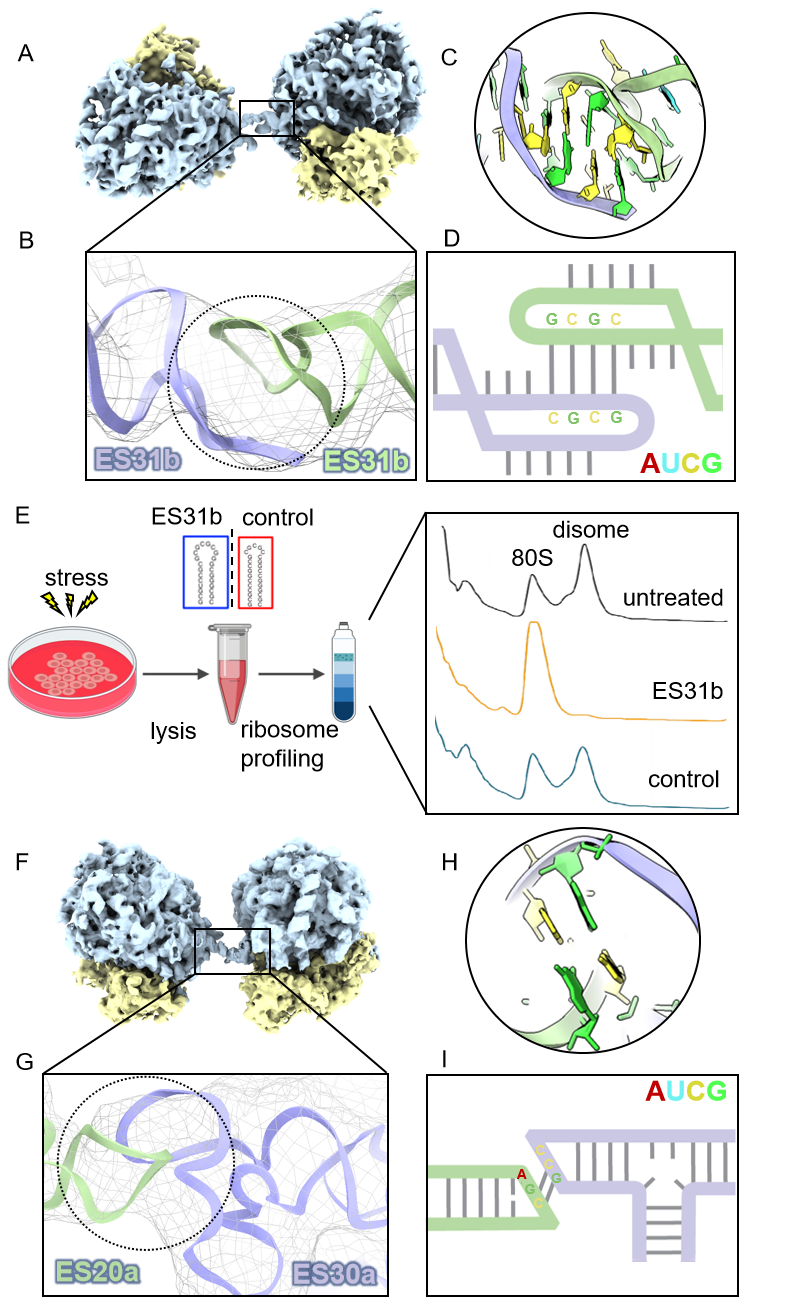
图1:rRNA扩展片段介导的核糖体二聚化机制。A–D. 核糖体rRNA扩展片段ES31b介导二聚体的形成。E. RNA竞争实验验证二聚体相互作用界面;F–I. 核糖体rRNA扩展片段ES30a和ES20a介导的另一类二聚体形成。
综上,本研究确立了rRNA扩展片段在应激诱导核糖体休眠二聚化过程中的核心作用,拓展了对翻译调控机制的认识。不同于原核细胞依赖休眠因子实现核糖体失活与储存的方式,真核细胞可直接利用核糖体自身的rRNA元件,实现快速且可逆的应激响应,为理解翻译调控的空间组织原则提供了新的视角。


