这种新G-四链体的结构特征是在G-quartet平面上含有G-空缺,它可以从环境中吸收一个含Guanine碱基的分子而形成一个更加稳定的结构。这种被命名为GVBQ(G-vacancy-bearing G-quadruplexes,G-空缺G-四链体)的G-四链体可以在单链核酸和转录的双链DNA中形成。它具有响应原核和真核细胞的生理浓度的GMP和GTP的能力并可以籍此而影响DNA聚合酶的DNA复制活性。生物信息学分析发现这类结构在原核和真核基因中有特殊的分布规律,提示它们可以在细胞中形成并与基因表达调控有关。该项研究已于2015年在线发表在PNAS(论文链接)。
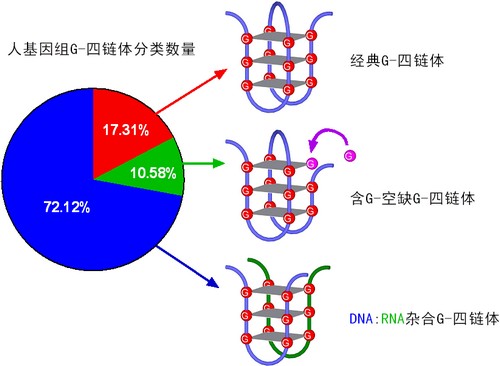
与经典G-四链体相比,研究组所发现的DNA:RNA杂合G-四链体和含G-空缺G-四链体具有的独特性质是它们能够响应生理过程或生理状态,进而进行相关调控。例如DNA:RNA杂合G-四链体在转录中形成又反过来调节转录活性。含G-空缺G-四链体可能通过响应GMP和GTP的生理浓度而感知细胞的代谢状态,改变调节能力。根据目前的统计,研究组所发现的DNA:RNA杂合G-四链体和含G-空缺G-四链体数量在人基因组占到了三种G-四链体的80%以上。这两种新G-四链体的生理响应能力和数量表明它们是人基因组中具有更大生理调控潜能的主流G-四链体结构。
在G-四链体其它方面研究组亦获得两项进展。博士生吴壬乙同学在活细菌中检测到了DNA:RNA杂合G-四链体的形成和它对转录造成的中断,并发现杂合G-四链体相对于经典G-四链体是导致转录中断的主要因素。这一发现表明杂合G-四链体可以在活细胞中形成并具有干预细胞转录活性的能力。该工作于2015年发表于Angew Chem Int Ed(论文链接)。