并被该刊编辑部选为本周PNAS新闻发布会推介论文(见附图、附录A)。
病变导致中脑多巴胺神经元的丢失和相应大脑纹状体DA的减少是PD的一种典型病理特征。1990年《新英格兰医学杂志》报道,将人源胚胎DA神经元干细胞移植到病人纹状体成功实现PD的治疗。但是这种策略遇到胚胎伦理问题无法推广。2011年起美国加州大学张康、丁盛等应用小分子成功诱导人源干细胞定向分化成为DA神经干细胞并实现在体外大规模增殖,点燃了对应用“DA干细胞”治疗PD的期待。但是,在科学上必须首先解决两个基本问题,一是移植的DA干细胞到体内能有治疗效果吗?二是移植的干细胞能够在纹状体分泌DA吗?
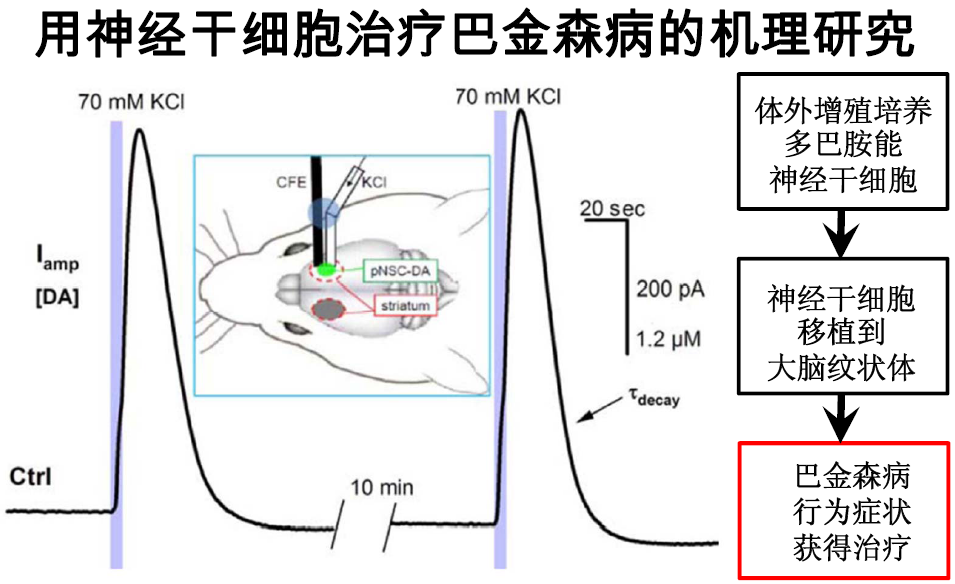
周专组首次联合两种在体(in vivo)检测技术,实现原位鉴定和记录DA分泌信号。 一是基于在体微透析的高效液相色谱大鼠大脑纹状体HPLC技术, 以原位定性分析DA分泌; 二是电化学微碳纤维电极技术, 以原位定量实时记录DA分泌。 结果证明移植人源DA干细胞16周后动物PD行为改善,与此前报道一致。更为重要的是,他们首次证明此时的DA干细胞直接分泌DA。这项转化医学的突破性进展应用了周专1994年发明、20年来不断改良的电化学低噪音微碳纤维电极技术,为今后的其他干细胞治疗机理研究提供了在体验证干细胞功能的范例。
本项研究在周专实验室完成。体外分化、增殖人源DA干细胞由美国加州大学张康、第二军医大学李文林合作完成。第一作者康新江是分子医学研究所博士研究生。受到科技部973和基金委项目、北大-清华联合生命中心、生物膜国家重点实验室、麦戈文脑研究所资助。
附录A:PNAS Journalist Summary:
Researchers report that grafted neural stem cells may partially reverse the symptoms of Parkinson’s disease in rats via the direct release of dopamine into a part of the forebrain known as the striatum. Loss of dopaminergic neurons and a corresponding decline in dopamine release are hallmark signs of Parkinson’s disease. Previous studies have explored the use of cell-replacement therapy using dopamine-like neurons generated from self-renewable primitive neural stem cells. But it remains unclear whether this strategy can fully restore dopamine levels in the striatum, and whether the dopamine is released by the transplanted neurons or by the surrounding healthy cells in the striatum. Zhuan Zhou and colleagues demonstrate that grafted neural stem cells directly release dopamine in the damaged striatum in vivo and partially rescue a rat model of Parkinson’s disease. The authors combined two existing methods—microdialysis-based high-performance liquid chromatography (HPLC) and nafion-coated carbon fiber electrodes (CFE)—to identify the released substance as dopamine and locate the site of its release in the rat striatum. The findings revealed that dopamine release and reuptake by the grafted neurons reduced abnormalities related to the progression of Parkinson’s disease and alleviated symptoms of the disease in rats. According to the authors, the findings provide proof-of-concept evidence to potentially support future clinical translation.





